
- 연구실 소개
연구실 소개
C1 가스 리파이너리 사업단
이화여자대학교 박진병 교수님 연구실 (식품생물공학연구실)
연구실 개요
박진병 교수 연구실에서는 효소공학/합성생물학/대사공학 기반으로 다양한 고부가 소재 생합성을 위한 고성능 생촉매 구축 및 생물전환 기술을 연구 개발 중에 있다. 지난 10 년 동안 지방/지방산으로부터 의약품/식품/화장품 및 바이오플라스틱 제조에 활용 가능한 다양한 기능성 소재의 생합성 기술을 연구하여 Angewandte Chemie International Edition, ACS Catalysis 등의 국제 저널에 다수의 논문을 게재하였고, 미국, 일본, 중국, EU에 국제특허를 등록하였다 (3장. 대표 연구성과 참조).
최근에는 전남대 김정선교수 연구실과 공동으로 C1/C2 화합물로부터 C2 이상의 고부가 소재 생합성을 위한 신규 효소 탐색, 구조 기반 효소반응 메카니즘 규명, 효소구조재설계, 신규 생물전환 경로 구축, 생촉매 개발 등을 연구하고 있다.
주요 연구내용 소개
(1) Biotransformation을 이용한 지방/지방산의 고부가 기술 개발
지방/지방산은 자연계에 널리 존재하고 있으나 식용유로 주로 사용되고 있고, 바이오디젤 등의 연료/케미컬 생산에 제한적으로 사용되고 있다. 본 연구실에서는 재생 가능한 지방/지방산으로부터 효소공학/합성생물학/대사공학 기술을 바탕으로 ω-hydroxycarboxylic acid, ω-aminocarboxylic acid, α,ω-dicarboxylic acid, long-chain aliphatic amines, long-chain aliphatic esters 등과 같은 고부가 소재 생합성 기술을 연구하고 있다 (3장. 대표 연구성과 참조).
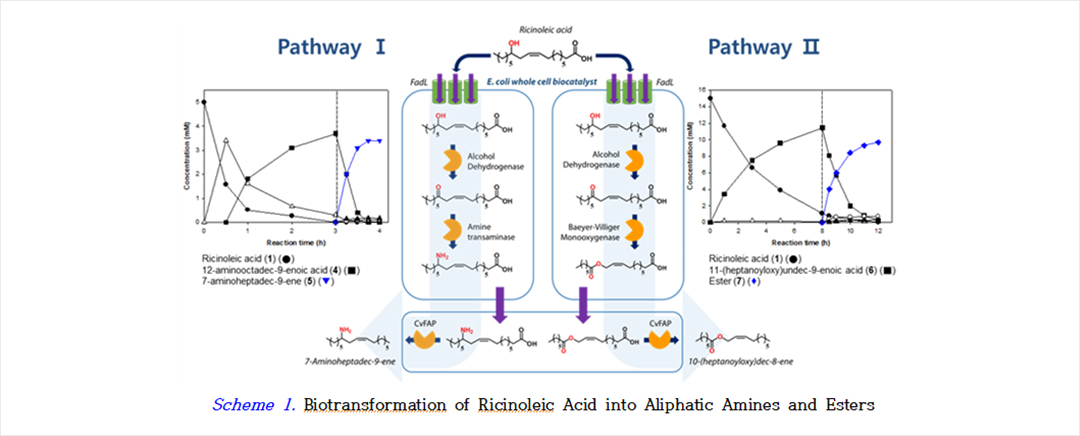
한 가지 예로 피마자 기름의 주성분인 리시놀레산으로부터 대장균 기반의 전세포 생촉매를 이용하여 long-chain aliphatic amines와 중쇄지방산의 전구체인 long-chain aliphatic esters를 고수율로 생합성하는 연구를 수행하였고 (Scheme 1, Figure 1 참조), 연구 결과들은 2020년 Angewandte Chemie International Edition에 발표되었다.

(2) Biotransformation을 위한 고성능 생촉매 개발
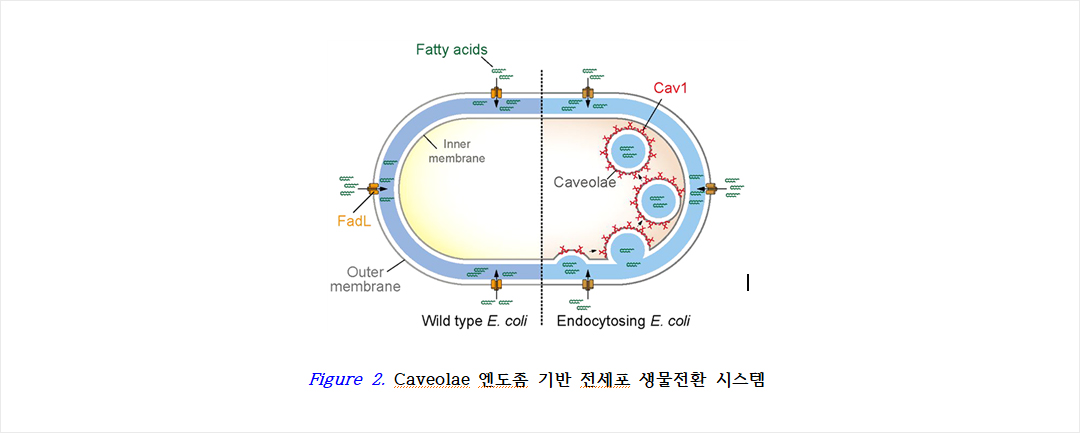
지방산이나 폴리페놀과 같은 소수성 유기화합물의 생물전환, 특히 수산화기를 도입하는 생물전환을 위한 전세포 촉매 개발에 대한 연구를 수행하고 있다. 반응 기질과 반응 산물에 대하여 내성이 높고 반응에 필요한 보효소(NAD(P)H)를 효율적으로 재생하고 반응 기질이나 반응 산물의 transport 효율이 높은 생촉매 개발에 대한 연구를 수행하고 있다. 한 가지 예로 대장균에 Caveolae 엔도좀 형성을 유도하여 지방산의 수송 및 내성을 향상시켰고 (Figure 2 참조), 연구 결과들은 2019년 ACS Synthetic Biology에 발표되었다.
또한 산화반응 중 일어나는 다양한 생물전환 효소들의 불활성화 메커니즘을 규명하기 위하여 모델링과 시뮬레이션 방법을 이용하고 이를 기반으로 산화 안정성 및 열 안정성과 반응 활성 향상을 위한 효소 engineering도 수행하고 있다.
(3) C-C 결합 생성용 효소/생촉매 개발 연구
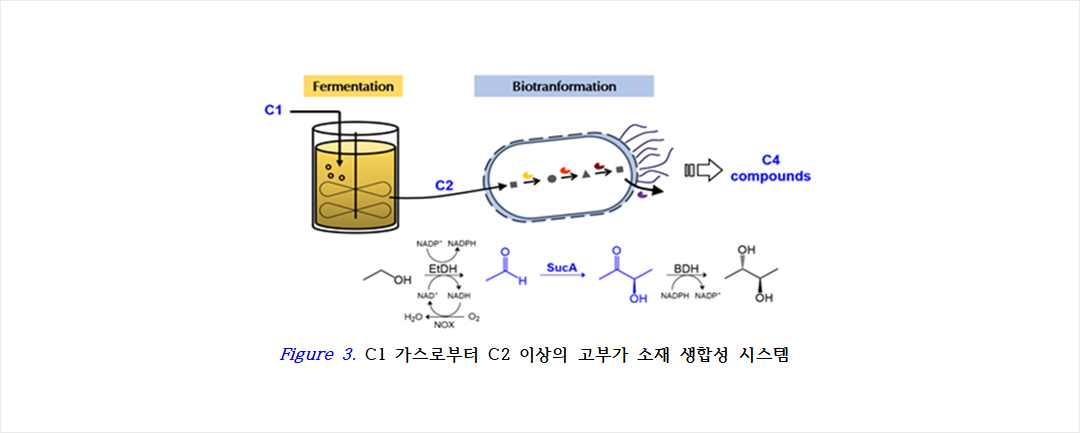
C2 화합물인 아세트알데하이드로부터 C4 화합물인 R-특이적 아세토인을 생산하기 위해 C-C 결합 생성 활성을 가진 효소군의 라이브러리를 구축하였으며, 구조 및 반응 특성을 조사하여 생물전환속도가 빠르고 높은 광학활성을 보이는 효소를 선별하였다 (Figure 3 참조). 또한 효소/단백질 구조 분석 전문가인 김정선교수 연구실과의 공동연구를 통해 새로운 효소의 3차 구조와 효소 활성 자리를 결정하였고 이를 기반으로 C2 전환용 효소 반응 메커니즘을 규명하였다. 연구 결과들은 2020년 Catalysis Science & Technology에 발표되었다.
C1 가스의 고부가화를 위한 신규 C-C 결합 생성용 효소 및 생물전환 시스템도 연구하고 있다. 최근 김정선교수 연구실과의 공동연구를 통해 C1 화합물인 포름알데하이드로부터 C2 화합물인 글리코알데하이드를 선택적으로 생합성 할 수 있는 신규 효소를 확보하였고, 이를 활용한 C1 화합물로부터 glycolic acid 생합성을 연구하고 있다. 또한, C1 가스로부터 C2 이상의 고부가 소재를 고속으로 생산하기 위한 엔도좀/엑소좀 기반의 새로운 생물전환 시스템 개발도 연구하고 있다.
대표 연구 성과
1. Cha, H.-J., S.-Y. Hwang, D.-S. Lee, R. K. Akula, Y.-U. Kwon, M. Voß, E. Schuiten, U. Bornscheuer, F. Hollmann, D.-K. Oh, and J.-B. Park. Photoenzymatic cascade transformation of renewable fatty acids into long chain aliphatic amines and esters. Angew. Chem. Int. Ed., In press. DOI: 10.1002/anie.201915108.
2. Seo, P.-W., H.-J. Jo, I. Y. Hwang, H.-Y. Jeong, J.-H. Kim, J.-W. Kim, E. Y. Lee, J.-B. Park, and J.-S. Kim. Understanding the molecular properties of the E1 subunit (SucA) of α-ketoglutarate dehydrogenase complex from Vibrio vulnificus for the enantioselective ligation of acetaldehydes into (R)-acetoin. Catal Sci. Technol., 10:79-85 (2020.01).
3. Song, J.-W., J.-H. Seo, D.-K. Oh, U. T. Bornscheuer, and J.-B. Park. Design and engineering of whole-cell biocatalytic cascades for the valorization of fatty acids. Catal Sci. Technol., 10:46-64 (2020.01).
4. Seo, E.-J., H.-J. Kim, M.-J. Kim, J.-S. Kim, and J.-B. Park. Cofactor specificity engineering of a long chain secondary alcohol dehydrogenase from Micrococcus luteus for redox-neutral biotransformation of fatty acids. Chem. Commun., 55: 14462-14465 (2019.12).
5. Seo, E.-J., C.W. Kang, J.-M. Woo, S. Jang, Y. J. Yeon, G. Y. Jung, and J.-B. Park. Multi-level engineering of Baeyer-Villiger monooxygenase-based Escherichia coli biocatalysts for the production of C9 chemicals from oleic acid. Metab. Eng., 54:137–144 (2019.07).
6. Shin, J., J. Yu, M. Park, C. Kim, H. Kim, Y. Park, Y.-H. Song, C.-S. Shin, K. H. Chung, J.-B. Park, and D.-H. Kweon. Endocytosing Escherichia coli as a whole-cell biocatalyst of fatty acids. ACS Synth. Biol., 8:1055-1066 (2019.04).
7. Lee, D.-S., J.-W. Song, M. Voß, E. Schuiten, A. R. Kumar, Y.-U. Kwon, U. Bornscheuer, and J.-B. Park. Enzyme cascade reactions for the biosynthesis of long chain aliphatic amines from renewable fatty acids. Adv. Synth. Catal., 361:1359-1367 (2019.03).
8. Woo, J.-M., E.-Y. Jeon, E.-J. Seo, J.-H. Seo, D.-Y. Lee, Y. -J. Yeon, and J.-B. Park. Improving catalytic activity of the Baeyer–Villiger monooxygenase based Escherichia coli biocatalysts for the overproduction of (Z)-11-(heptanoyloxy)undec-9-enoic acid from ricinoleic acid. Sci. Rep., 8:10280 (2018.07).
9. Seo, E.-J., Y.J. Yeon, J.-H. Seo, J.-H. Lee, J.P. Boñgol, Y. Oh, J.M. Park, S.-M. Lim, C.-G. Lee, J.-B. Park. Enzyme/whole-cell biotransformation of plant oils, yeast derived oils, and microalgae fatty acid methyl esters into n-nonanoic acid, 9-hydroxynonanoic acid, and 1,9-nonanedioic acid. Biores. Technol., 251:288-294 (2018.03).
10. Cha, H.-J., E.-J. Seo, J.-W. Song, H.-J. Jo, A. Ravi Kumar, J.-B. Park. Simultaneous enzyme/whole-cell biotransformation of C18 ricinoleic acid into (R)-3-hydroxynonanoic acid, 9-hydroxynonanoic acid, and 1,9-nonanedioic acid. Adv. Synth. Catal., 360:696-703 (2018.02).
연구실 구성원

박진병교수 연구실은 포스닥 1명, 연구원 1명, 석박사 통합과정 4명, 석사과정 8명으로 구성되어 있다. 최근 2017년부터 현재까지 진행한 대표 연구 성과는 SCI 급 논문 24건, 특허등록 3건 등 우수한 성과를 통하여 효소공학/생물전환 분야에서 대표 선두 주자로 나아가고 있다.


